產品與研發PRODUCTS & RD
Meta 1(癌症轉移藥物開發平台)
癌症的致死率高,無外乎因為控制不了癌細胞的轉移,進而擴散至全身而導致多重器官衰竭,因此在癌症的研究領域裡,發現如何控制或者影響癌症轉移的機制,便成為癌症新藥開發研究的重要問題,如果了解到癌症如何轉移並且開發出具有療效的藥物,以後的癌症將不會再造成人類的死亡就如同發現了聖經中的(聖杯),人類的長生不老將不再是夢想。
信力生技藉由本身所開發出的動物平台(Orthotopic/Metastatic Cell Line-Derived Xenograft, CDX Models),透過次世代基因定序分析方式找出一個特定的排列組合,當擁有這一系列的排列組合基因可以使正常的細胞癌化且具備轉移能力,在小鼠模型研究中得到了證實,其中Meta1此一基因角色在腫瘤細胞中扮演著關鍵性角色。
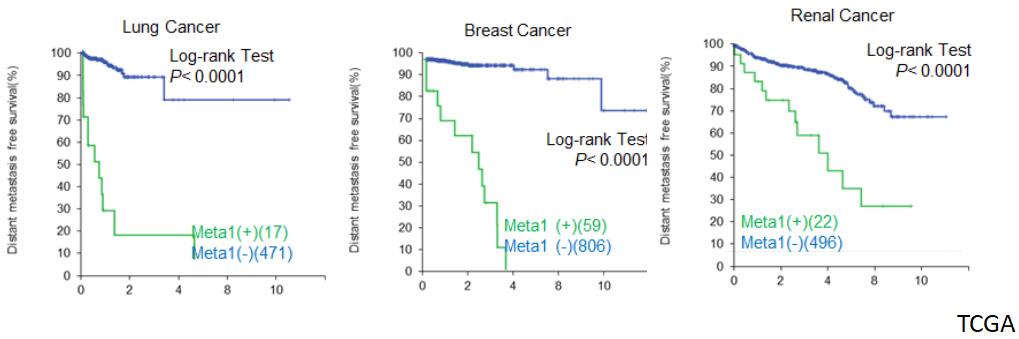
藉由此一系列的研究平台,信力生技已掌握Meta1調控癌細胞轉移的分子機制,也藉由此一調控系統發現,腫瘤細胞在得到Meta1基因調控下使得代謝方式改變,更能適應在血液循環中存活達到遠端轉移。信力生技依據此特性發展出有效的藥物報導系統,藉由當細胞在代謝過程中酸鹼的改變將產生不同螢光,當前導藥物或單株抗體能夠抑制Meta1基因功能時,螢光顏色將出現改變,跳脫傳統藥物篩選中只能透過細胞是否死亡作為依據,能更有效精準化的針對癌細胞特有的蛋白功能做為毒殺系統,以達到精準化醫學的目的。
近年來在國際藥物研發市場最熱門的話題便是『Antibody Drug Conjugate (ADC)』技術,利用抗體連結小分子藥物,透過抗體的標靶性將小分子藥物帶至病灶,ADC技術則能結合抗體與小分子藥物的優點;藥效顯著的小分子藥物在有了抗體這個導彈後,便能憑藉著抗體的標靶性準確地傳輸至癌細胞處,利用抗體與癌細胞上特殊受體結合的特性,「登陸」於癌細胞上,並誘使癌細胞將聯結於抗體上的抗癌藥物「吞噬」至細胞內後,讓藥物得以從癌細胞內部釋放藥效,繼而消滅癌細胞。正因為ADC技術讓抗癌療效佳的小分子藥物也有了標靶傳輸的特性,近年來許多生技大廠亦紛紛投注於此領域的研究。根據Azoth Analytics分析指出ADC藥物,預計在2017至2022年間將以21.82%的年均複合增長率強勢增長,也使得癌症治療有更廣泛的治療方向。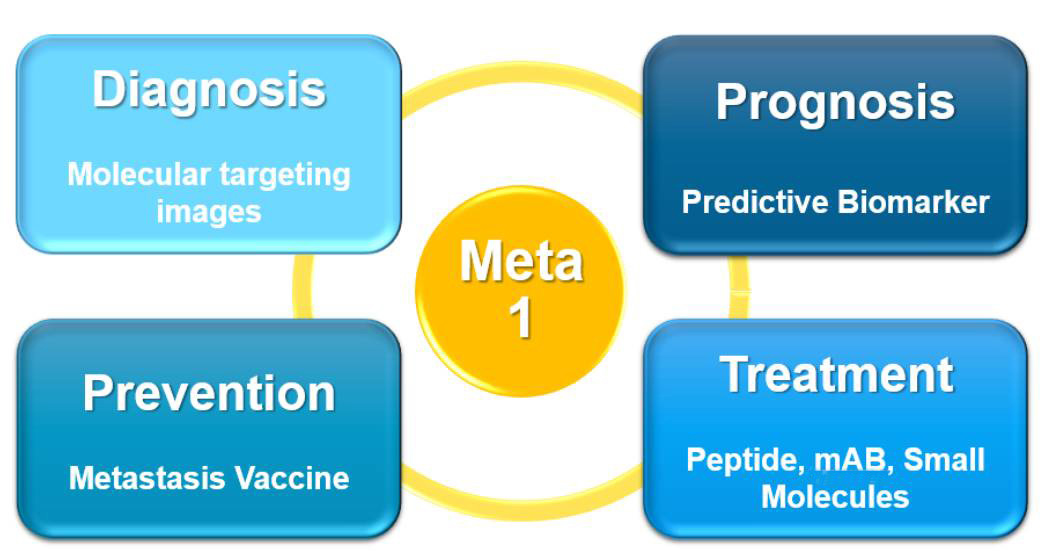
由於ADC本身便是一個結合了抗體、連接體與小分子藥物的平台,只要掌握其中的技術門檻,便可運用此平台結合不同的抗體與小分子藥物,來發展各種不同的藥物。信力生技目前也積極投入,將現有Meta1基因製成的單株抗體測試,進而製成ADC標靶藥物傳輸平台,之後導入小分子藥物進行包裹後與抗體連結作為未來發展新契機,且其市場潛力預估將可達世界各大藥廠過去合作案例之價值。
信力生技藉由本身所開發出的動物平台(Orthotopic/Metastatic Cell Line-Derived Xenograft, CDX Models),透過次世代基因定序分析方式找出一個特定的排列組合,當擁有這一系列的排列組合基因可以使正常的細胞癌化且具備轉移能力,在小鼠模型研究中得到了證實,其中Meta1此一基因角色在腫瘤細胞中扮演著關鍵性角色。

藉由此一系列的研究平台,信力生技已掌握Meta1調控癌細胞轉移的分子機制,也藉由此一調控系統發現,腫瘤細胞在得到Meta1基因調控下使得代謝方式改變,更能適應在血液循環中存活達到遠端轉移。信力生技依據此特性發展出有效的藥物報導系統,藉由當細胞在代謝過程中酸鹼的改變將產生不同螢光,當前導藥物或單株抗體能夠抑制Meta1基因功能時,螢光顏色將出現改變,跳脫傳統藥物篩選中只能透過細胞是否死亡作為依據,能更有效精準化的針對癌細胞特有的蛋白功能做為毒殺系統,以達到精準化醫學的目的。
近年來在國際藥物研發市場最熱門的話題便是『Antibody Drug Conjugate (ADC)』技術,利用抗體連結小分子藥物,透過抗體的標靶性將小分子藥物帶至病灶,ADC技術則能結合抗體與小分子藥物的優點;藥效顯著的小分子藥物在有了抗體這個導彈後,便能憑藉著抗體的標靶性準確地傳輸至癌細胞處,利用抗體與癌細胞上特殊受體結合的特性,「登陸」於癌細胞上,並誘使癌細胞將聯結於抗體上的抗癌藥物「吞噬」至細胞內後,讓藥物得以從癌細胞內部釋放藥效,繼而消滅癌細胞。正因為ADC技術讓抗癌療效佳的小分子藥物也有了標靶傳輸的特性,近年來許多生技大廠亦紛紛投注於此領域的研究。根據Azoth Analytics分析指出ADC藥物,預計在2017至2022年間將以21.82%的年均複合增長率強勢增長,也使得癌症治療有更廣泛的治療方向。
Personalized and Precision Medicine

由於ADC本身便是一個結合了抗體、連接體與小分子藥物的平台,只要掌握其中的技術門檻,便可運用此平台結合不同的抗體與小分子藥物,來發展各種不同的藥物。信力生技目前也積極投入,將現有Meta1基因製成的單株抗體測試,進而製成ADC標靶藥物傳輸平台,之後導入小分子藥物進行包裹後與抗體連結作為未來發展新契機,且其市場潛力預估將可達世界各大藥廠過去合作案例之價值。